11/12/2024
En el vasto e invisible universo subatómico, los electrones son los protagonistas de una danza perpetua alrededor del núcleo atómico. Pero, ¿cómo se organizan? ¿Qué rige su movimiento? Y, más importante aún, ¿cómo podemos calcular la energía que poseen en cada uno de sus intrincados niveles? Estas preguntas han fascinado a científicos durante siglos, y su comprensión es fundamental para desentrañar los secretos de la materia y la energía.
Desde los primeros modelos atómicos, la estructura interna del átomo ha sido un campo de intenso debate y descubrimiento. Las teorías iniciales, como el modelo del “pudín de pasas” de J.J. Thomson, o el revolucionario descubrimiento del núcleo por Ernest Rutherford, sentaron las bases para una comprensión más profunda. Sin embargo, fue la visión audaz de Niels Bohr a principios del siglo XX la que transformó radicalmente nuestra percepción de cómo los electrones se comportan dentro del átomo, introduciendo la revolucionaria idea de la cuantificación de la energía.
- El Modelo de Bohr y la Cuantificación de la Energía
- La Fórmula de la Energía del Electrón: Desentrañando el Misterio
- Cálculo de la Energía en Transiciones Electrónicas
- ¿Cuántos Electrones Caben en Cada Nivel de Energía?
- Importancia y Aplicaciones de los Niveles de Energía
- Resumen de Fórmulas Clave
- Preguntas Frecuentes (FAQ)
El Modelo de Bohr y la Cuantificación de la Energía
Antes de Bohr, se pensaba que los electrones podían orbitar el núcleo en cualquier trayectoria, de manera similar a como los planetas giran alrededor del sol, pero esto no explicaba la estabilidad de los átomos ni los espectros de emisión discretos. La gran contribución de Bohr fue postular que los electrones solo pueden existir en órbitas o "capas" específicas y discretas, cada una con un radio fijo y una energía asociada. Es decir, la energía de un electrón dentro de un átomo no es continua, sino que está cuantificada: solo puede tomar ciertos valores permitidos, como si subiera y bajara escalones en una escalera, sin poder detenerse entre ellos.
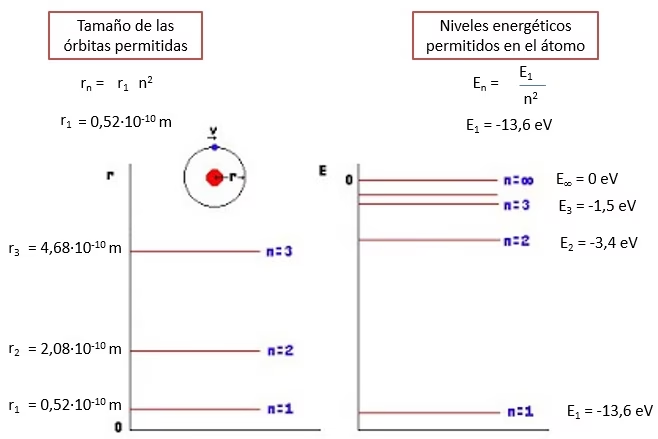
En el modelo de Bohr para el átomo de hidrógeno, se asumió que solo se permitían aquellas órbitas con un radio específico, dado por la siguiente ecuación:
r(n) = n² × r(1)
Donde r(n) es el radio de la órbita en el nivel de energía n, y r(1) es el radio de la primera órbita (el estado fundamental del hidrógeno), también conocido como el radio de Bohr, aproximadamente 0.0529 nanómetros. La variable n representa el número cuántico principal (1, 2, 3…), que designa el nivel de energía principal. Es imposible que los electrones existan entre estas capas permitidas, lo que explica la sorprendente estabilidad de los átomos.
La Fórmula de la Energía del Electrón: Desentrañando el Misterio
Una vez establecida la idea de las órbitas cuantificadas, Bohr procedió a calcular la energía de un electrón en el nivel n del átomo de hidrógeno. Considerando los electrones en órbitas circulares y cuantificadas, la fórmula para la energía de un electrón en un nivel n es la siguiente:
E(n) = - (1/n²) × 13.6 eV
En esta ecuación, E(n) representa la energía del electrón en el enésimo nivel de energía. El valor de 13.6 eV (electronvoltios) es de suma importancia, ya que corresponde a la energía más baja posible de un electrón de hidrógeno, es decir, la energía del estado fundamental E(1). El signo negativo en la fórmula indica que el electrón está ligado al núcleo; se necesita energía para sacarlo del átomo (para ionizarlo).
Esta fórmula nos permite calcular la energía de un electrón en cualquier nivel de energía principal para un átomo de hidrógeno. Por ejemplo, para el primer nivel (n=1), la energía es -13.6 eV. Para el segundo nivel (n=2), la energía es -13.6 eV / 2² = -13.6 eV / 4 = -3.4 eV. Como se puede observar, a medida que n aumenta (el electrón se aleja del núcleo), la energía se vuelve menos negativa, lo que significa que el electrón está menos fuertemente unido al núcleo y su energía es mayor (menos energía de enlace).

Cálculo de la Energía en Transiciones Electrónicas
Los electrones no permanecen estáticos en sus niveles de energía. Pueden saltar de un nivel a otro, un proceso que es fundamental para la interacción de la materia con la luz. Cuando un electrón absorbe energía, generalmente en forma de fotones (partículas de luz), puede "excitarse" y saltar a un nivel de energía superior, también conocido como estado excitado. Sin embargo, este estado es inherentemente menos estable.
Dado que la naturaleza tiende hacia la estabilidad, un electrón excitado no permanece en un nivel de energía superior por mucho tiempo. Rápidamente "caerá" de nuevo a un nivel de energía más bajo y más estable, emitiendo la energía sobrante en forma de un nuevo fotón. La energía de este fotón emitido (o absorbido) es equivalente a la diferencia exacta de energía entre los dos niveles de energía involucrados en la transición. Esta energía se puede calcular utilizando la siguiente ecuación:
hv = ΔE = (1/n_low² - 1/n_high²) × 13.6 eV
Aquí, hv representa la energía del fotón (donde h es la constante de Planck y v es la frecuencia de la luz), ΔE es el cambio en la energía, n_low es el número cuántico del nivel de energía inferior, y n_high es el número cuántico del nivel de energía superior. Esta ecuación es la base para entender los espectros de emisión y absorción de los átomos, que son como las "huellas dactilares" de cada elemento químico.
La fórmula general para definir los niveles de energía, aplicable no solo a transiciones sino a la energía total de un nivel, se puede expresar como:
E = E₀ / n²
Donde E₀ es 13.6 eV (para el hidrógeno) y n es 1, 2, 3, y así sucesivamente.
¿Cuántos Electrones Caben en Cada Nivel de Energía?
Una pregunta frecuente, y crucial para entender la configuración electrónica de los átomos, es cuántos electrones pueden ocupar cada uno de estos niveles de energía. Aunque el modelo de Bohr se centra en la energía, el marco de la mecánica cuántica que lo sucedió nos proporciona una regla clara para la capacidad máxima de electrones por nivel principal.
Cada nivel de energía principal, denotado por el número cuántico n (n=1, 2, 3, etc.), puede albergar un número máximo de electrones. Esta capacidad se determina mediante la fórmula:
Número máximo de electrones = 2n²
Veamos algunos ejemplos:
- Para el primer nivel de energía (n=1):
2 × (1)² = 2 × 1 = 2electrones. - Para el segundo nivel de energía (n=2):
2 × (2)² = 2 × 4 = 8electrones. - Para el tercer nivel de energía (n=3):
2 × (3)² = 2 × 9 = 18electrones. - Para el cuarto nivel de energía (n=4):
2 × (4)² = 2 × 16 = 32electrones.
Esta regla, aunque no directamente derivada de las fórmulas de energía de Bohr, es fundamental para comprender la estructura de la tabla periódica y cómo los átomos forman enlaces químicos. Los electrones llenan estos niveles de energía en un orden específico, lo que determina las propiedades químicas de cada elemento.
Importancia y Aplicaciones de los Niveles de Energía
La comprensión de los niveles de energía de los electrones es mucho más que un ejercicio teórico; es la piedra angular de gran parte de la química y la física modernas. Permite explicar:
- Los Espectros Atómicos: Los colores específicos de luz que emiten o absorben los átomos son el resultado directo de las transiciones electrónicas entre niveles de energía definidos. Esto se utiliza en espectroscopia para identificar elementos, tanto en laboratorios como en estrellas distantes.
- La Formación de Enlaces Químicos: La forma en que los átomos interactúan y forman moléculas depende en gran medida de los electrones en sus niveles de energía más externos (electrones de valencia).
- El Funcionamiento de la Tecnología Moderna: Desde los láseres (que se basan en la emisión estimulada de fotones por electrones que regresan a niveles de energía más bajos) hasta los semiconductores en nuestros dispositivos electrónicos, los principios de los niveles de energía son omnipresentes.
- La Estabilidad de la Materia: La existencia de niveles de energía discretos es lo que impide que los electrones "caigan" en espiral hacia el núcleo, asegurando la estabilidad de los átomos y, por extensión, de toda la materia que conocemos.
Resumen de Fórmulas Clave
Para su referencia, aquí le presentamos un resumen de las fórmulas fundamentales discutidas:
| Concepto | Fórmula | Descripción |
|---|---|---|
| Radio Atómico (Modelo de Bohr, H) | r(n) = n² × r(1) | Radio de la órbita permitida para el nivel n. |
| Energía del Electrón (Nivel n, H) | E(n) = - (1/n²) × 13.6 eV | Energía de un electrón en el nivel n del átomo de hidrógeno. |
| Energía de Transición (Emisión/Absorción) | hv = ΔE = (1/n_low² - 1/n_high²) × 13.6 eV | Energía de un fotón absorbido o emitido durante una transición. |
| Fórmula General Niveles de Energía | E = E₀ / n² | Define la energía de los niveles para un átomo de un solo electrón (E₀ = 13.6 eV para H). |
Preguntas Frecuentes (FAQ)
¿Qué es un nivel de energía en un átomo?
Un nivel de energía es una región o capa específica alrededor del núcleo atómico donde los electrones tienen una cantidad de energía fija y definida. Los electrones no pueden tener cualquier valor de energía, sino solo los permitidos por estos niveles cuantificados.

¿Por qué los electrones no caen al núcleo?
Según la mecánica clásica, un electrón en órbita debería perder energía y caer en espiral hacia el núcleo. Sin embargo, el modelo de Bohr y la mecánica cuántica explican que los electrones solo pueden ocupar niveles de energía discretos y estables. No pueden perder energía continuamente ni "caer" por debajo de su nivel de energía más bajo (el estado fundamental) porque no hay niveles de energía inferiores disponibles.
¿Qué sucede cuando un electrón absorbe energía?
Cuando un electrón absorbe una cantidad de energía específica (generalmente un fotón con la energía exacta), salta a un nivel de energía superior, conocido como estado excitado. Este estado es temporal e inestable.
¿Es la fórmula de Bohr aplicable a todos los átomos?
La fórmula de Bohr para la energía y el radio es estrictamente precisa solo para átomos de un solo electrón, como el hidrógeno o iones hidrogenoides (por ejemplo, He⁺, Li²⁺). Para átomos con múltiples electrones, las interacciones entre ellos hacen que el cálculo sea mucho más complejo, y se requiere una descripción más avanzada de la mecánica cuántica.
¿Cómo se relacionan los niveles de energía con la tabla periódica?
Los niveles de energía son fundamentales para la organización de la tabla periódica. El número de electrones en el nivel de energía más externo (electrones de valencia) determina las propiedades químicas de un elemento y su posición en la tabla. Los periodos de la tabla periódica corresponden al número de niveles de energía ocupados por los electrones de un átomo.
La exploración de los niveles de energía de los electrones es una ventana a la comprensión de cómo funciona el universo a su nivel más fundamental. Desde la cuantificación de la energía propuesta por Bohr hasta la regla de la capacidad máxima de electrones por nivel, cada concepto nos acerca más a desvelar los misterios que rigen la materia que nos rodea y de la que estamos hechos. Este conocimiento no solo es un triunfo intelectual, sino también la base para innumerables avances tecnológicos que moldean nuestro mundo.
Si quieres conocer otros artículos parecidos a Desentrañando la Energía Electrónica del Átomo puedes visitar la categoría Física.

